Новые тренировочные варианты статград по химии 9 класс формат ОГЭ 2024 задания и ответы с решением для подготовки к реальному экзамену, который пройдёт у 9 класса 27 мая 2024 года в понедельник. Каждый пробник соответствует структуре варианта КИМ экзамена ФИПИ. Работа состоит из двух частей, включающих в себя 24 задания. Часть 1 содержит 19 заданий с кратким ответом, часть 2 содержит 5 заданий с развёрнутым ответом. На выполнение тренировочной работы по химии отводится 3 часа (180 минут).
Варианты статград по химии 9 класс ОГЭ 2024
-
Варианты ХИ2390101-ХИ2390104 ОГЭ по химии
-
Варианты ХИ2390201-ХИ2390204 ОГЭ по химии
-
Варианты ХИ2390301-ХИ2390304 ОГЭ по химии
-
Варианты ХИ2390401-ХИ2390404 ОГЭ по химии
-
Варианты ХИ2390501-ХИ2390504 ОГЭ по химии
Ответы к заданиям 1–19 записываются в виде последовательности цифр (чисел) или числа. Ответ запишите в поле ответа в тексте работы. К заданиям 20–23 следует дать полный развёрнутый ответ, включающий в себя необходимые уравнения реакций и расчёты. Задания выполняются на чистом листе бумаги. Задание 24 предполагает выполнение эксперимента под наблюдением учителя. К выполнению задания 24 следует приступать после выполнения обучающимся задания 23 и не ранее чем через 30 минут после начала выполнения работы.
Работа выполняется яркими чёрными чернилами. Допускается использование гелевой или капиллярной ручки. При выполнении работы Вы можете пользоваться Периодической системой химических элементов Д.И. Менделеева, таблицей растворимости солей, кислот и оснований в воде, электрохимическим рядом напряжений металлов и непрограммируемым калькулятором.
Баллы и оценки за ОГЭ 2024 по химии
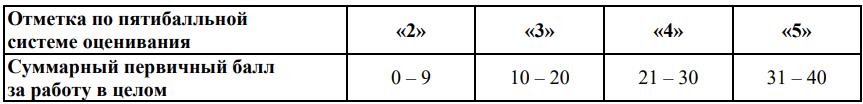
Максимальное количество первичных баллов, которое может получить участник ОГЭ за выполнение всей экзаменационной работы, – 40 баллов. Шкала перевода суммарного первичного балла за выполнение экзаменационной работы в отметку по пятибалльной системе оценивания. Рекомендуемый минимальный первичный балл для отбора обучающихся в профильные классы для обучения по образовательным программам среднего общего образования – 27 баллов.
Сложные задания с вариантов ФИПИ
Задание 1. Вычислите в процентах массовую долю меди в халькопирите. Запишите число с точностью до десятых. При расчёте используйте целочисленные атомные массы элементов.
Задание 2. Одним из главных потребителей меди является машиностроение. Один автомобиль с двигателем внутреннего сгорания состоит из деталей, для изготовления которых расходуется 21 кг чистой меди. Для получения меди использовали 3 тонны халькопирита (CuFeS2). На сколько автомобилей может быть израсходована полученная медь? Запишите число с точностью до целых.
Задание 3. Вычислите объём углекислого газа (н. у.), который выделится при действии на избыток карбоната кальция 730 г 20 %-ной соляной кислоты. В ответе запишите уравнение реакции, о которой идёт речь в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Задание 4. Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата меди(II), и укажите признаки их протекания (запах газа, цвет осадка или раствора).
Задание 5. С какими из перечисленных ниже веществ оксид кальция вступает в реакцию соединения?
1) кислород
2) водород
3) вода
4) углекислый газ
5) соляная кислота
Задание 6. Выберите два вещества, при полной диссоциации 1 моль которых образуется 2 моль катионов.
1) фосфат калия
2) сульфит натрия
3) хлорид кальция
4) карбонат аммония
5) сульфат цинка
Задание 7. Вычислите массовую долю (в процентах) хрома в хромистом железняке. Запишите число с точностью до десятых.
Задание 8. В нержавеющей стали, применяемой для изготовления одного комплекта кастрюль, содержится 641 г хрома. Сколько комплектов кухонной посуды может быть изготовлено из нержавеющей стали, полученной из 13,8 кг хромистого железняка (FeO. Cr2O3)? Запишите число с точностью до целых.
Задание 9. При взаимодействии металлического натрия с водой образовалось 100 г раствора гидроксида натрия и 1,12 л водорода. Вычислите массовую долю гидроксида натрия в растворе.
Задание 10. Из перечисленных суждений о приготовлении растворов и правилах работы с веществами выберите верное(-ые). 1) При приготовлении раствора серной кислоты следует порции концентрированной кислоты постепенно приливать к воде. 2) Вода выветривается из кристаллов медного купороса, поэтому для получения чистого CuSO4∙5H2O необходимо старый реактив растворить в воде, а затем провести кристаллизацию. 3) Поглощение газообразного аммиака водой необходимо проводить под тягой. 4) Для лабораторного получения 30%-го раствора пероксида водорода проводят кипячение продающегося в аптеке 3%-го раствора пероксида. Запишите в поле ответа номер(-а) верного(-ых) суждения(-й).
Задание 11. Один пакетик суспензии лекарственного препарата Фосфалюгель (Phosphalugel) содержит 2,48 г фосфата алюминия (AlРО4). При лечении заболевания пациент принимает препарат по 2 пакетика 3 раза в сутки после еды. Вычислите массу алюминия в граммах, поступающую в организм человека за сутки. Запишите число с точностью до десятых.
Задание 12. Через раствор гидроксида натрия пропустили 4,48 л сернистого газа (н. у.). Образовалось 126 г раствора сульфита натрия. Вычислите массовую долю соли в полученном растворе.
Задание 13. Для получения хорошего урожая перед посадкой картофеля в почву вносят доломитовую муку (CaCO3 . MgCO3) из расчёта 3 г магния на 1 м2 . Для обогащения почвы магнием в почву внесли 9,23 кг доломитовой муки, других удобрений не применялось. Вычислите площадь участка в м2 . Запишите число с точностью до целых.
Прочитайте текст и выполните задания 23 и 24. Для ответа на задание 23 используйте чистый лист. Запишите сначала номер задания (23), а затем развёрнутый ответ к нему. Ответ записывайте чётко и разборчиво. Задание 24 выполняйте только под наблюдением учителя. При выполнении задания 24 или сразу после выполнения можно делать записи в черновике, после чего нужно вернуться к выполнению других заданий тренировочной работы до момента окончания отведённого на выполнение работы времени.

