Новый пробный тренировочный вариант №21 по химии 11 класс в формате ЕГЭ 2022 новые задания с ответами и решением в формате реального ЕГЭ 2022 по химии из открытого банка тренировочных вариантов ФИПИ со всем изменениями 2022 года.
Скачать вариант ЕГЭ 2022 по химии
ЕГЭ 2022 по химии тренировочный вариант №21 задания с ответами
егэ2022_химия_11класс_вариант21_ответыОтветы и решения для варианта
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
- 1) Fe
- 2) Ca
- 3) P
- 4) Mn
- 5) As
1)Определите, атомы каких из указанных в ряду элементов образуют ион, содержащий 23 электрона.
Ответ: 14
2)Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в главных подгруппах. Расположите выбранные элементы в порядке увеличения их атомного радиуса. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Ответ: 352
3)Из числа указанных в ряду элементов выберите два элемента, высшая валентность которых равна (V).
Ответ: 35
4)Из предложенного перечня выберите два вещества, в которых присутствует водородная связь.
- 1) триэтиламин
- 2) формальдегид
- 3) бутанол-2
- 4) иодоводород
- 5) фтороводород
Ответ: 35
5)Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите: А) соль слабой кислоты, Б) кислотный оксид, В) кислоту, соответствующую хлорату натрия.
Ответ: 352
6)К одной из двух пробирок, содержащих гидроксид стронция, добавили раствор соли Х, а к другой – раствор слабого электролита Y. В результате в каждой из пробирок наблюдали выпадение белого осадка. Определите вещества X и Y, которые могут вступать в описанные реакции.
- 1) CuCl2
- 2) KHCO3
- 3) H2SO4
- 4) HF
- 5) Fe(NO3)3
Ответ: 24
9)Задана следующая схема превращений веществ: Na2O2 ଡ଼→ Na2O → NaOH → Y → CuCl2. Определите, какие из указанных веществ являются веществами X и Y.
- 1) Na
- 2) CuSO4
- 3) O2
- 4) CuO
- 5) Cu(OH)2
Ответ: 15
11)Из предложенного перечня выберите два вещества, молекулы которых содержат ровно шесть σсвязей.
- 1) этанол
- 2) уксусная кислота
- 3) циклогексан
- 4) пропин
- 5) метиламин
Ответ: 45
12)Выберите все вещества, которые можно получить из ацетилена в одну стадию.
- 1) этаналь
- 2) этиленгликоль
- 3) циклогексан
- 4) оксалат калия
- 5) винилхлорид
Ответ: 145
13)Из предложенного перечня выберите два вещества, которые являются более слабыми основаниями, чем анилин.
- 1) диметиламин
- 2) дифениламин
- 3) триэтиламин
- 4) трифениламин
- 5) изопропиламин
Ответ: 24
17)Из предложенного перечня выберите все реакции замещения
- 1) нитрование бензола
- 2) взаимодействие хлорэтана со спиртовым раствором щелочи
- 3) растворение оксида лития в воде
- 4) взаимодействие сероводорода с бромной водой
- 5) реакция фенола с гидроксидом калия
Ответ: 14
18)Из предложенного перечня выберите все факторы, которые увеличивают скорость реакции, протекающей по схеме: Fe3O4 (тв.) + 4С(тв.) = 3Fe(тв.) + 4CO(г)
- 1) повышение площади поверхности соприкосновения реагентов
- 2) повышение температуры
- 3) понижение давления
- 4) понижение концентрации угарного газа
- 5) повышение давления
Ответ: 12
26)К 10%-ному раствору соли добавили некоторое количество этой же соли и получили 300 г 19%- го раствора. Вычислите массу соли (в граммах), добавленной к исходному раствору. В ответ запишите целое число.
Ответ: 30
27)Теплота образования 1 моль воды из кислорода и водорода равна 286 кДж/моль. Вычислите, сколько тепла выделится при образовании 1,44 г воды. Ответ запишите в кДж с точностью до сотых.
Ответ: 22,88
28)При взаимодействии 10,27 г перманганата калия с избытком концентрированной соляной кислоты выделилось 10,65 г газа. Вычислите выход газа в процентах от теоретически возможного. Ответ округлите до десятых.
Ответ: 92,3
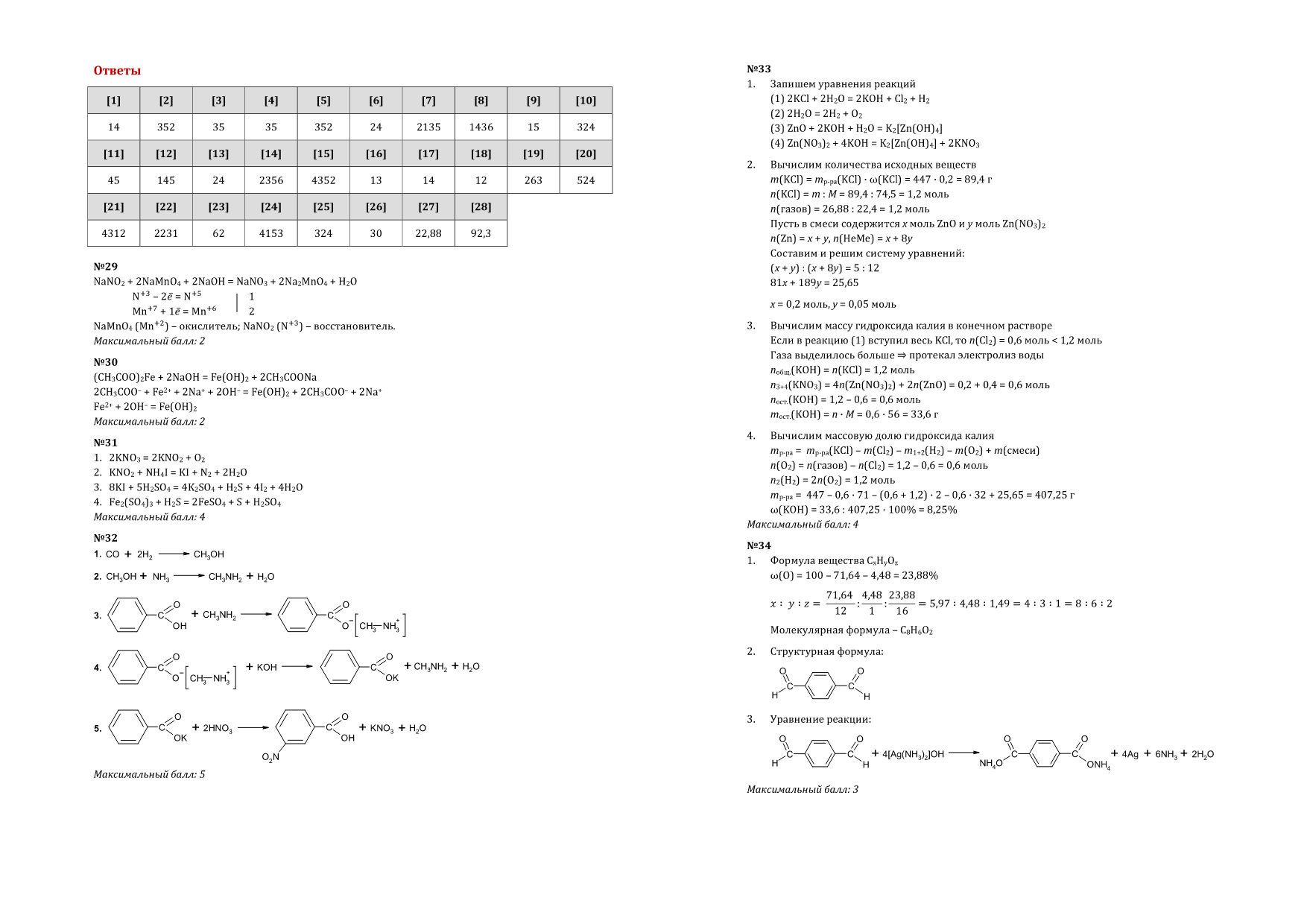
29)Из предложенного перечня выберите вещества, между которыми в щелочной среде протекает окислительно-восстановительная реакция. В ходе этой реакции число принятых электронов оказалось два раза меньше числа отданных электронов (в расчете на одну формульную единицу реагента). Запишите уравнение реакции с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня выберите вещества, между которыми протекает реакция ионного обмена с образованием осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с использованием выбранных веществ.
31)Нитрат калия подвергли термическому разложению. Твердый остаток поместили в раствор иодида аммония, полученную смесь нагревали до прекращения выделения газа. Образовавшуюся в ходе реакции соль выделили и обработали концентрированной серной кислотой. Выделившийся в ходе реакции газ с неприятным запахом пропустили через раствор сульфата железа (III) и наблюдали появление светло-желтого осадка. Составьте уравнения четырех описанных реакций.
33)447 г 20%-го раствора хлорида калия подвергли электролизу (с инертными электродами). Процесс остановили, когда на аноде выделилось 26,88 л (при н.у.) газов. К полученному после электролиза раствору добавили 25,65 г смеси оксида и нитрата цинка, в которой на 5 атомов металла приходится 12 атомов неметаллов. Вычислите массовую долю гидроксида калия в конечном растворе.
34)Неизвестное органическое вещество А содержит 71,64% углерода, 4,48% водорода и еще один элемент. Известно, что оно не вступает в реакцию присоединения с бромной водой, но реагирует с аммиачным раствором оксида серебра в мольном соотношении 1 : 4. Функциональные группы в молекуле А расположены на максимальном удалении друг от друга. На основании данных в задаче: 1. Проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества А; 2. Составьте структурную формулу неизвестного вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3. Напишите уравнение реакции органического вещества с избытком аммиачного раствора оксида серебра, используя структурную формулу вещества.